COVID-19 : « Ce virus est très futé. Il frappe une molécule qui nous protège »
Un récepteur qui est la porte d’entrée du virus dans les cellules agit de façon importante sur l'évolution des patients et pourrait être à la base d'un traitement.
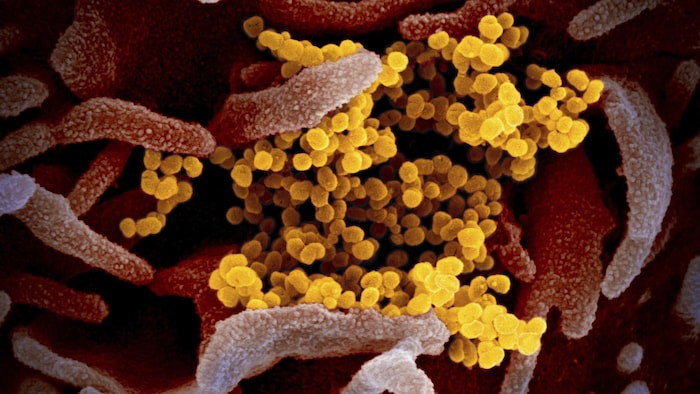
Image captée au microscope de coronavirus SRAS-CoV-2 (en jaune), à la surface de cellules cultivées en laboratoire (en rose foncé).
Photo : La Presse canadienne / AP/NIAID-RML
Prenez note que cet article publié en 2020 pourrait contenir des informations qui ne sont plus à jour.
Considérée à l’origine comme une maladie strictement respiratoire, la COVID-19 est de plus en plus comprise, dans les cas graves, comme étant une maladie systémique qui affecte de nombreux tissus et organes. Voici l'état des connaissances.
Dans la foulée de l’épidémie du SRAS au milieu des années 2000, Josef Penninger avait, avec ses collègues, mis le doigt sur un récepteur présent dans la membrane de nos cellules, connu depuis quelques années, qui possède de multiples fonctions, mais qui constitue aussi la porte d’entrée des coronavirus dans nos cellules.
Il s’agit d’ACE2, l’enzyme de conversion de l’angiotensine II. Une protéine à la surface du virus, appelée protéine S, s’amarre au récepteur ACE2 de concert avec d’autres molécules, ce qui permet au virus de pénétrer dans nos cellules et d’entamer son cycle d’infection.
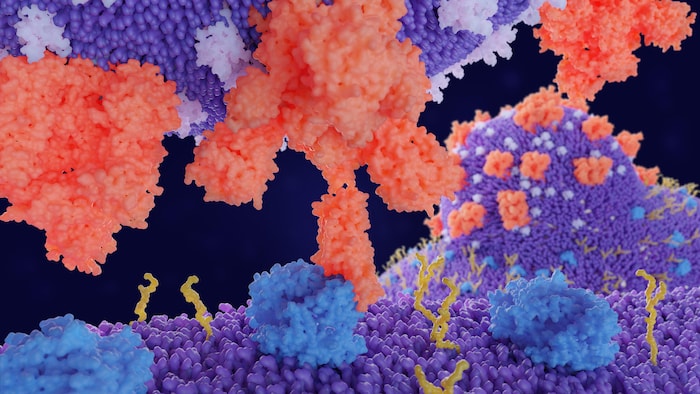
Une protéine S du coronavirus (en rose) s'amarre à un récepteur ACE2 d'une cellule humaine (en bleu), ce qui permet au virus de pénétrer dans la cellule.
Photo : iStock / selvanegra
C’est le même mécanisme que pour d’autres coronavirus, que ce soit ceux qui circulent parmi nous couramment et qui donnent un banal rhume ou d'autres très dangereux comme celui du SRAS en 2003 ou encore le SRAS-CoV-2 cette année, rappelle le chercheur et professeur de médecine à l’Université de la Colombie-Britannique.
Mais dans le cas actuel du SRAS-CoV-2, qui cause la COVID-19, la protéine S du virus qui s'amarre au récepteur ACE2 le fait de façon particulièrement efficace, ce qui pourrait expliquer la force
de ce nouveau coronavirus. Des chercheurs ont en effet montré en mars dernier que le SRAS-CoV-2 a de 10 à 20 fois plus d’affinité pour le récepteur ACE2 que le SRAS.
Du nez, aux poumons, au système sanguin
Un grand avantage pour le virus de passer par ACE2 est que ce récepteur se retrouve à peu près partout dans notre corps.
D’abord ACE2 est très présent dans notre nez et dans notre gorge. Si je vous contamine avec mes gouttelettes, c’est là que ça va commencer. En conséquence, les gens vont tousser, avoir mal à la tête, mais souvent, ça va s’arrêter là
, illustre Josef Penninger.
Mais ACE2 est aussi exprimé sur des cellules dans nos poumons. Alors le virus peut s’y propager, et à peu près 20 % des gens développent une pneumonie et des symptômes graves
, poursuit-il.
L’inflammation s’aggrave et certains vaisseaux peuvent-être endommagés. C’est là que le virus peut passer au sang et infecter tout notre système, poursuit-il.
L’intérieur de nos vaisseaux, formé d’une mince couche de cellules appelée endothélium, est lui aussi tapissé de récepteurs ACE2, qui constituent autant de voies d’accès pour le virus.
L’endothélium, c'est la structure, la surface interne des vaisseaux sanguins et lymphatiques. Son rôle est d'offrir une surface qui ne soit pas coagulante, qui ne favorise pas la formation de caillots. Elle imperméabilise les vaisseaux et les rend non thrombogènes
, explique le Dr George-Étienne Rivard, hémato-oncologue au CHU Sainte-Justine.
Or, les cellules de l’endothélium infectées par le virus meurent et sont décollées de la paroi. En dessous, il y a ce qu'on appelle le facteur tissulaire : il active de façon très importante la coagulation sanguine. Alors, avec la dénudation de la paroi vasculaire, il y a formation de microcaillots et de thromboses. Et les cellules qui étaient tributaires de vaisseaux sanguins pour leur apport en nutriments et en oxygène ne sont plus nourries
, poursuit le Dr Rivard.
C’est ce qui expliquerait les microcaillots observés un peu partout dans le corps chez des patients aux soins intensifs qui ont subi des complications de la COVID-19.
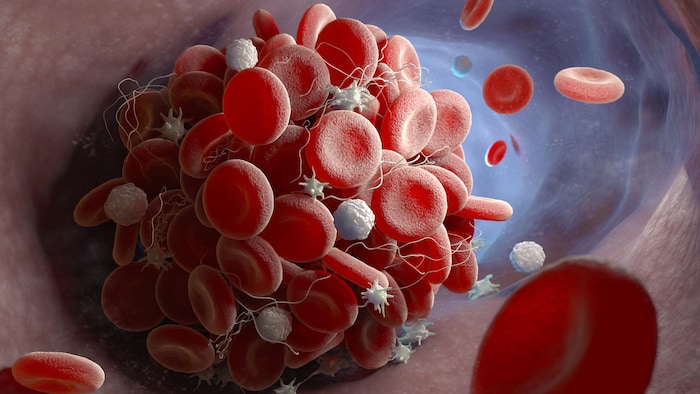
La formation de caillots sanguins qui bloquent la circulation sanguine est une complication fréquente chez les patients COVID-19.
Photo : getty images/istockphoto / iLexx
La réaction inflammatoire
De plus, avec la mort cellulaire et la coagulation, il y a aussi l’activation des voies métaboliques qui conduisent à la production de cytokines, ces protéines agentes du système immunitaire, explique le Dr Rivard. C’est la réaction inflammatoire qui est enclenchée et qui sert à protéger notre corps contre les agressions, mais qui peut s’emballer chez certaines personnes, ce qui constitue la fameuse tempête inflammatoire.
La réaction inflammatoire peut provoquer de la vasoconstriction (le resserrement des vaisseaux) ou de la vasodilatation (la dilatation des vaisseaux), poursuit le Dr Rivard. Si on a, par exemple, un environnement où beaucoup de microvaisseaux ont été bloqués par des microcaillots, et qu'en plus se présente une cytokine inflammatoire qui est vasoconstrictante, le peu d'apport en oxygène et en nutriments qu'on réussissait encore à acheminer au tissu à cause des microthromboses va être davantage compromis par une vasoconstriction.
Conséquence : le tissu meurt.
Cela expliquerait en partie les défaillances d’organes constatées chez bon nombre de patients gravement atteints, particulièrement chez ceux qui ont déjà des maladies préexistantes qui fragilisent les vaisseaux, comme le diabète et les maladies cardiovasculaires.
Pour ce qui est des poumons, non seulement les échanges gazeux sont-ils compromis à cause du pus qui s’accumule dans les bronches et les alvéoles en raison de l’infection, mais aussi à cause de l’apport sanguin qui est grandement diminué dans les stades avancés de la maladie.
Alors, les bronches sont bloquées, il n’y a pas d'entrée d'oxygène, pas de sortie de CO2. Les vaisseaux sont bloqués par des caillots, pas d'entrée d'oxygène, pas de sortie de CO2. Et à un moment donné, le respirateur ne suffit plus, et on meurt.
Aussi, ACE2 est exprimé dans plusieurs autres tissus et organes, ce qui complique encore la situation.
Le virus peut ainsi infecter directement les reins, le coeur, les intestins, parce qu’on retrouve ACE2 à tous ces endroits (Nouvelle fenêtre). De récentes recherches parlent de symptômes neurologiques (Nouvelle fenêtre), et on retrouve ACE2 dans le cerveau
, cite le Dr Penninger.
Dans les derniers stades, ce n’est plus une maladie pulmonaire, mais bien une maladie systémique qui touche plusieurs organes. Alors, ACE2 explique probablement toute la distribution de la maladie, des tissus qui sont infectés.
Un rôle régulateur et protecteur perdu
Les Drs Penninger et Rivard expliquent qu’ACE2 est au coeur d’un système hormonal, appelé rénine-angiotensine, connu depuis des décennies, qui régule notre pression artérielle et la bonne marche de notre métabolisme.
Or, lorsque le virus se lie au récepteur ACE2, il l’empêche de surcroît d’accomplir sa tâche normale, ce qui vient perturber l’équilibre du système rénine-angiotensine, explique Josef Penninger. Il se produit alors une accumulation de l’hormone peptidique angiotensine II, qui a un grand effet vasoconstricteur, ce qui peut contribuer à aggraver des symptômes, comme provoquer d’importants problèmes cardiovasculaires.
Nous savons par nos recherches qu’ACE2 protège les poumons et beaucoup d’autres tissus des dommages. Mais lorsque le virus se lie à ACE2, son rôle est compromis; la protection qu’il offrait est perdue, et la maladie empire. Donc, vous enlevez ACE2, et les maladies des poumons, du coeur, des vaisseaux sanguins et des reins s’aggravent
, dit le Dr Penninger.
Ce virus est très "futé". Il frappe une molécule qui nous protège. Et c’est pourquoi il y a autant de tissus touchés par la COVID-19 et que cette maladie est si grave.
Étudier l'effet des hormones androgènes
Par ailleurs, l’expression d’ACE2 et d’une autre molécule qui facilite l’arrimage du virus aux cellules, la protéase transmembranaire à sérine 2 (TMPRSS2), est favorisée entre autres par les hormones androgènes, comme la testostérone. Certains chercheurs pensent que cela pourrait expliquer en partie pourquoi les hommes sont proportionnellement plus nombreux que les femmes à développer des symptômes graves de la COVID-19 – car ils produisent plus d’androgènes et donc plus d’ACE2 et de TMPRSS2 –, et aussi pourquoi les enfants, qui produisent peu d’hormones androgènes, sont moins touchés par la maladie. Mais cela demeure des pistes de recherche (Nouvelle fenêtre).
Le Dr Rivard rappelle que beaucoup d’autres facteurs peuvent contribuer à la surreprésentation des hommes chez les patients COVID-19 graves, comme les comorbidités plus présentes chez les hommes ou encore les différences comportementales – le tabagisme est plus fréquent chez les hommes, par exemple. Il faut aussi tenir compte du polymorphisme, soit les petites différences entre les individus pour un gène donné, qui font que, même exposés à un niveau semblable d’androgènes, deux personnes peuvent avoir des réactions tout à fait différentes.
Des connaissances fondamentales aux traitements
En ce moment, beaucoup de recherches sur des traitements ou des vaccins potentiels visent ce couple formé de la protéine S du virus et du récepteur ACE2.
Probablement entre 40 % et 50 % de toute la recherche qui a cours en ce moment sur des médicaments ou des vaccins se concentre spécifiquement sur cette interaction entre le virus et ACE2.
Le Dr Penninger fait partie d’une équipe qui teste en ce moment une molécule, qui est en fait une enzyme ACE2 modifiée que l’on injecte dans l’organisme. Celle-ci sert en quelque sorte de leurre
, pour que le coronavirus s’y attache, au lieu de s’arrimer aux récepteurs ACE2 à la surface des cellules.
Nous avons montré dans un article récent (Nouvelle fenêtre) que l’on arrive [en laboratoire] à réduire d’un facteur de 1000 à 5000 fois la charge virale. En plus, la molécule permet au système rénine-angiotensine de retrouver son équilibre
, dit le Dr Penninger.
L'équipe recrute en ce moment des centaines de patients COVID-19 dans plusieurs pays pour tester l'efficacité de cette molécule chez les personnes gravement atteintes.
Le chercheur se fait humble, rappelant que des centaines de traitements différents sont en train d’être testés à l’heure actuelle.
Il faut faire les études correctement. Il faut savoir si les médicaments fonctionnent ou non contre la COVID-19.